por amhei | Jan 30, 2018 | Espanol
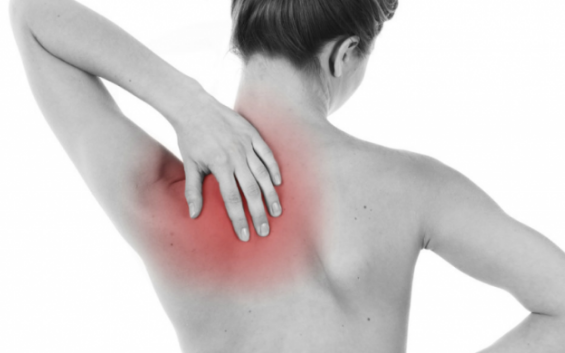
La Fibromialgia (FM) es una enfermedad que se caracteriza por un cuadro de dolor musculo esquelético crónico y generalizado de origen desconocido, donde no existen otras enfermedades o alteraciones que lo expliquen. La FM es una patología reconocida por todas las...
por amhei | Jan 25, 2018 | Espanol
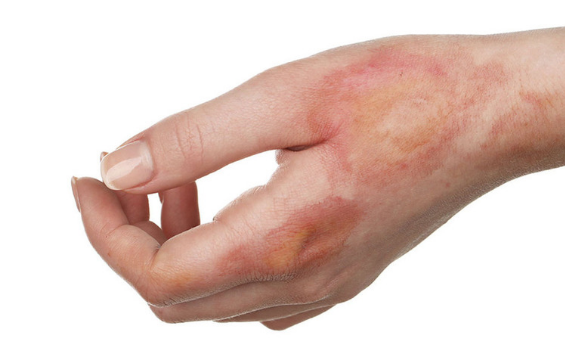
Los primeros trabajos que demuestran la eficacia de TOHB como adyuvante en el tratamiento de las quemaduras surgieron hace más de 50 años en mineros tratados por intoxicación con monóxido de carbono dónde se evidenció un aceleramiento en la cicatrización de sus...
por amhei | Jan 3, 2018 | Espanol
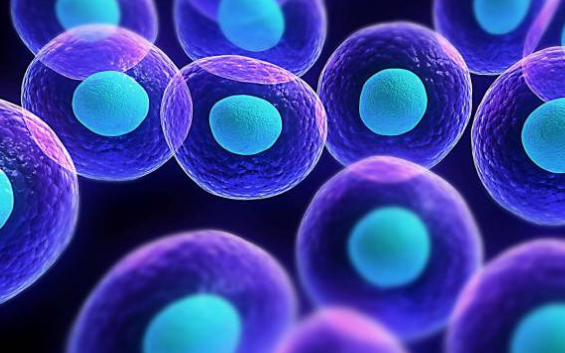
Las células madres o células progenitoras (SPCs) de los adultos exhiben propiedades similares a las células embrionarias y son muy prometedoras para el tratamiento de desórdenes degenerativos. Se han encontrado en muchos órganos y tejidos, incluyendo cerebro, médula...

por amhei | Jan 3, 2018 | Espanol
El Oxígeno es el elemento vital que sostiene la vida humana. Cada célula del cuerpo lo necesita para completar los procesos metabólicos que dan vida y energía al organismo. Hace muchos años, estudiando este elemento natural, se desarrolló el principio de la...





